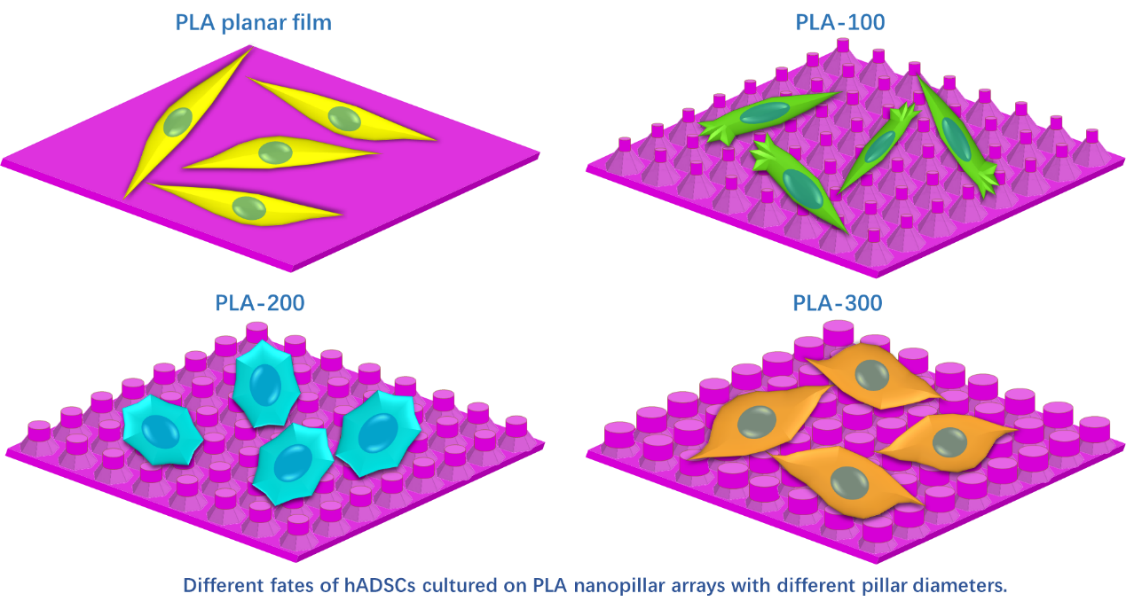
近日,山东大学晶体材料国家重点实验室刘宏教授和刘铎教授以及山东大学齐鲁医院刘超博士提出了一种简便易行的骨组织修复材料制备方法,并研究了聚乳酸纳米阵列的纳米柱直径变化对人脂肪来源干细胞成骨分化的影响及纳米柱阵列在体内的异位成骨效果,这项工作为骨修复提供了一个重要的结构参数,并推进了纳米结构材料在体内的应用。相关研究成果以“Polylactic Acid Nanopillar Array-Driven Osteogenic Differentiation of Human Adipose-Derived Stem Cells Determined by Pillar Diameter(聚乳酸纳米柱阵列的纳米柱直径对人脂肪来源干细胞成骨分化的调控)”为题,发表在国际著名期刊Nano Letters(DOI: 10.1021/acs.nanolett.7b04747;影响因子:12.712)上。文章第一作者为山东大学晶体材料国家重点实验室2015级硕博连读博士研究生张珊,通讯作者为刘宏教授、刘铎教授和山东大学齐鲁医院刘超博士,山东大学为第一作者单位。
骨缺损导致患者运动障碍、功能缺失甚至危及生命。由于自体骨的来源有限,异体骨有排异性,骨修复与再生一直是医学难题。以干细胞、支架材料和生长因子为主要构成元素的组织工程方法是这一难题的最有前途的解决方式。其中,调控干细胞向成骨细胞分化,是实现新骨形成、骨组织重建的关键。利用特殊蛋白对干细胞分化进行调控的方法,因蛋白价格来源少、价格高、容易失活,且调控耗周期长,难以实用化。刘宏教授团队结合前人研究,一直致力于利用材料表面纳米结构来实现可靠、快速、持久且位置可控的干细胞分化的精准调控,这种干细胞的物理调控方法为骨修复提供了重要的途径。刘宏教授课题组在纳米结构介导的成骨分化方面也已取得新的成果(ACS Appl. Mater. Interfaces 2017, 9, 33717−33727,DOI: 10.1021/acsami.7b13313;Acta Biomaterialia, 2018, DOI: 10.1016/j.actbio.2018.02.033)。
该研究工作得到了国家自然科学基金面上项目、国家重点研发计划重点专项和晶体材料国家重点实验室的支持。
相关链接:https://pubs.acs.org/doi/abs/10.1021/acs.nanolett.7b04747